Mientras siguen en curso las autorizaciones para las vacunas contra COVID-19 en la niñez, hace unos días la Organización Mundial de la Salud (OMS) instó a la población africana a aplicar la primera vacuna contra la malaria a los más afectados por el parásito Plasmodium falciparum: niños y niñas. La vacuna diseñada desde 2015 bajo el nombre de RTS,S/AS01 ha demostrado reducir las muertes por esta enfermedad y ser segura para la infancia.
Desde hace años es bien conocido que la peor versión de la malaria es transmitida en África, mata a más de 260 mil menores de cinco años anualmente en este continente. También se tenía información sobre los mecanismos que llevaban al mosquito a transmitir el paludismo (la otra forma en que se denomina a esta enfermedad), pero lograr una vacuna que protegiera a la población infantil tomó más de 30 años, mucha inversión, trabajo en equipo y una buena dosis de voluntad política.

La malaria tiene un impacto tan importante para África que incluso se han reportado(1) los efectos de las crisis epidémicas sobre la violencia civil en áreas con población adulta altamente susceptible al parásito, debido a que los brotes traen costos de tratamientos importantes para los hogares pobres y ausentismo laboral.
Por otra parte, el incremento de casos depende en gran parte del aspecto climático, pues aumenta la presencia de mosquitos en temporada de lluvias, así que la historia de la malaria también nos advierte sobre posibles consecuencias del cambio climático.
La recomendación(2) de la OMS se realiza luego de los resultados satisfactorios de dos programas piloto en los que se aplicó RTS,S/AS01 a 800 mil niñas y niños en Ghana, Kenia y Malawi durante un lapso de dos años, en dichos estudios se encontró que esta vacuna evitó cuatro de cada 10 casos de paludismo. El director general de la OMS, Tedros Adhanom señaló: “Al añadirla a las herramientas ya disponibles para prevenir el paludismo, podremos salvar la vida de decenas de miles de niños cada año”.

Zumbidos peligrosos
El paludismo es causado por el parásito plasmodium que se transmite a través de picaduras de mosquitos hembras infectadas del género Anopheles. Aunque hay más de 400 especies de Anopheles, solo 30 son importantes en temas de paludismo.
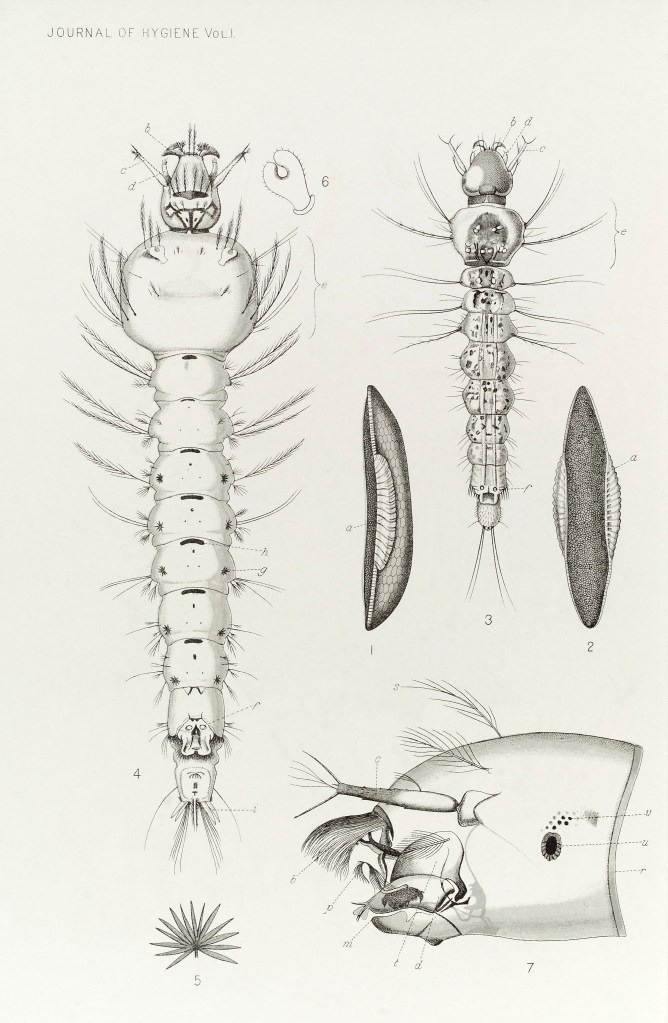
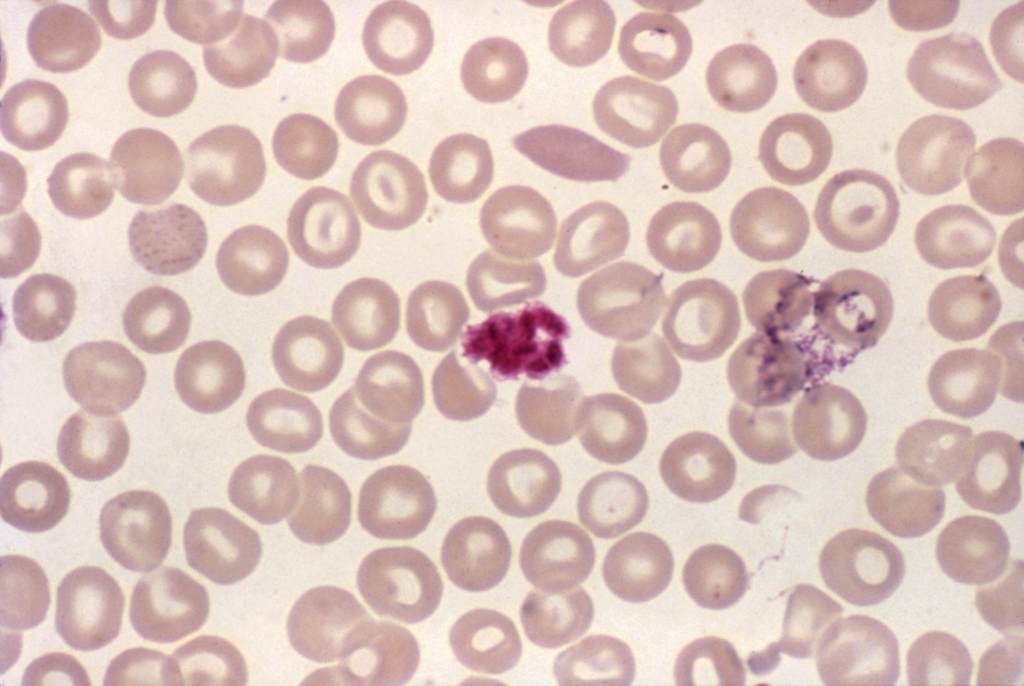
Las hembras son las únicas que se alimentan de sangre, es durante las picaduras que los mosquitos insertan a las personas su saliva con plasmodium. Después del piquete, los parásitos, llamados esporozoitos, viajan por el torrente sanguíneo hasta el hígado, ahí maduran y producen otra forma de parásitos, los merozoitos, estos ingresan al torrente sanguíneo e infectan a los glóbulos rojos causando la enfermedad.
Hay cinco especies de parásitos que causan la malaria, Plasmodium falciparum y Plasmodium vivax son las más peligrosas. Con la P. vivax, el diagnóstico es más esperanzador que con P. falciparum, pero el primero es más difícil de diagnosticar ya que “tiene la particularidad de producir recaídas porque los parásitos pueden almacenarse en el hígado y reactiva su desarrollo semanas o meses después”, explicó la investigadora del Centro Regional de Investigación en Salud Pública del Instituto Nacional de Salud Pública (INSP), Lilia González Cerón.
Aunque cuatro de las cinco especies de malaria no son objetivos para la vacuna RTS,S/AS01, actualmente estas responden bien al tratamiento actual, por ello es que la vacuna se enfocó en la malaria más mortífera.
La OMS indicó(3) que en 2019, P. falciparum fue la causa del 99.7 % ciento de los casos en África, 50 % de casos en Asia Sudoriental, 71 por ciento de los casos en la Región del Mediterráneo Oriental y 65% de la región Pacífico Occidental. Mientras que P. vivax es el parásito predominante en la Región de las Américas, donde es la causa del 75 % de los casos de paludismo.
Los mosquitos prefieren acumulaciones de agua para depositar sus huevos, y dado que la humedad juega un papel relevante en el número y supervivencia de los mosquitos, los charcos, piletas y cubetas en temporada de lluvias son focos importantes de malaria en los países tropicales.

La infección causa fiebre en la mayoría de los casos, además de dolor de cabeza y escalofríos, síntomas(4) que pueden presentarse entre los primeros 10 y 15 días después de la picadura, pero también llega a provocar intensos sudores y color amarillento en la piel, estos son secundarios a la destrucción de los glóbulos rojos por la invasión de los parásitos que inyecta el mosco. En las y los niños puede causar anemia grave y sufrimiento respiratorio que llevan a la muerte y en personas adultas afecta a distintos órganos.
Dificultades para una vacuna contra parásitos
La naturaleza del parásito fue retadora durante el diseño de una vacuna, pero también debe considerarse que las investigaciones para develar estos misterios se ven impactadas por el apoyo económico y político que se les da.
Respecto al desafío científico se tiene un microorganismo que es capaz(5) de adaptarse al huésped y escapar de las respuestas del sistema inmunitario. Durante años se buscaron proteínas que fueran candidatos capaces de inducir una fuerte respuesta inmunológica.
En la década de los setenta, explicó la especialista en parasitología médica, se identificó la proteína circumsporozoite que está en la superficie del esporozoito, es transmitida por los mosquitos e infecta al cuerpo humano. A esta proteína se le vio potencial porque recubre la superficie del parásito, entonces al desarrollar una respuesta de anticuerpos efectiva contra esta, se podría neutralizar al parásito y evitar que entre a su primera célula blanco.
Fue hasta la década de los ochentas cuando incrementó el apoyo político y económico de varias fuentes, con ello se logró construir esta vacuna y aunque antes se intentaron diferentes estrategias, con la mayoría encontraban grandes inconvenientes en sus respuestas o costos, entonces cada tanto se regresaba a circumsporozoite. Fue un ir y venir sobre esta proteína hasta que la empresa británica GlaxoSmithKline diseñó RTS,S/AS01, misma que recibió una opinión científica positiva de la Agencia Europea de Medicamentos (EMA) previo a su aplicación en población infantil.
Respecto a otras estrategias, Lilia González señaló que se revisó la posibilidad de tener una vacuna contra los parásitos que se desarrollan en la sangre, lo que no eliminaría la infección, pero reduciría la severidad de la enfermedad al bloquear la expansión del mismo. Un tercer blanco fueron las fases sexuales del parásito, «al atacarlas se interrumpiría la transmisión y la persona vacunada no sería foco de futuras infecciones porque en los mosquitos no se desarrollaría el parásito».
Lo que COVID-19 nos enseñó en temas de vacunas
La investigadora considera que esta vacuna tomó mucho tiempo por diversos factores, entre ellos el empezar a desarrollarse en un entorno más conservador respecto a la efectividad de las vacunas, pero sobre todo que el parásito tiene “moléculas muy polimórficas, es decir variables. En COVID-19 se habla de algunas variantes, pero en el caso del paludismo, en las regiones con alta transmisión, como en África, encontramos que cada individuo tiene una variante diferente”.
A esto se suma que “plasmodium falciparum cuenta con una proteína que se desarrolla en la superficie del esporozoito infectado y hace que el parásito sea secuestrado en los capilares y se esconda, por lo que no es alcanzado por herramientas diagnósticas, llegando a parecer negativo sin serlo, pero también se esconde de la respuesta inmune, esta proteína es muy variable, no se podría hacer una vacuna contra esta, pero se conoce esta peculiaridad del parásito que dificulta muchas cosas”.
La vacuna también demoró mucho por el asunto del porcentaje de protección, pues se pedía lo mismo que a las vacunas de las cartillas de vacunación que es de más del 90 por ciento, “sin embargo, cuando hablas de parásitos, tienes que cambiar la forma de pensar, no es como un virus, los parásitos son complejos, tienes que cambiar tus estándares, quizá se pueda tomar como buena señal que la vacuna sea capaz de que uno de cada dos niños infectado no muera”.
La doctora Lilia González explicó que el porcentaje de efectividad de RTS,S/A01 depende de los tiempos de aplicación, por ejemplo puede ser de 56 % a los 12 meses cuando se aplica refuerzo.
Esta vacuna estaba antes del COVID-19, pero la pandemia cambió la forma de pensar respecto a estas, “con SARS-CoV-2 se notó la necesidad de vacunas de uso de urgencia, eso hizo que se usarán tecnologías que antes no se permitían como de ARN que hoy funcionan. Se está abriendo el campo para mejorar y hacer otras vacunas con nuevas plataformas”.
Actualmente, acotó la investigadora, se tiene otra vacuna, la R21MM, que usa la misma proteína, pero introduce una parte más grande de la misma e induce una buena respuesta anticuerpos. En su primera evaluación clínica demostró que es capaz de proteger a más del 70 por ciento de la infancia, por ahora se sigue evaluando.
El caso de México
En 2019 hubo 229 millones de casos de paludismo en todo el mundo, de estos 409 mil resultaron en muertes y es notorio el problema de África cuando se sabe que 94 % de los casos y defunciones ocurrieron en ese continente, siendo las y los niños menores de cinco años más afectados pues en 2019 representaron 67 % de las muertes.
Aunque en zonas donde el paludismo es endémico, las personas adultas llegan a tener inmunidad parcial y con ello infecciones asintomáticas, no todos tienen la suerte de superar la enfermedad y en las primeras infecciones pueden desarrollar enfermedad severa, llegar al hospital y morir con mucha frecuencia. La niñez, las embarazadas, pacientes con VIH/sida, migrantes no inmunes de zonas endémicas, viajeros y población itinerante son los más vulnerables a la enfermedad grave.
Para México tenemos que bajaron los casos de 101 mil en el año 1989 a menos de 5 mil para 1997 y, aunque con el paso del huracán Paulina en 1997 se dio un repunte de casos, tres años después estos se redujeron 91 por ciento. Derivado de estas cifras ocurre otro fenómeno: que el tema no se investigue o comunique mucho. Respecto a esto, la científica Liliana González indicó: “Cuando teníamos más de 120 mil casos por año, se pensaba que no era importante estudiar el paludismo, ahora que hemos bajado a menos de mil casos por año, es más difícil hablar del tema”.
En México, la especie presente en los últimos 20 años es P. vivax, que produce recaídas debido a que los parásitos se quedan guardados en el hígado y se reactivan su desarrollo algunas semanas o meses después, Ante esto, la investigadora apuntó que las personas deben recibir un tratamiento completo para reducir esta tasa de recaídas al mínimo.

Respecto a esto, la OMS refirió(6) que en México, dos tercios de los estados mexicanos están libres de malaria desde el 2004, entre los que siguen con este problema destacan los pueblos indígenas que viven en regiones remotas en estados como Campeche, Chihuahua, Nayarit, Quintana Roo, Sinaloa, Sonora y Tabasco, así como Chiapas, donde se registran 81 por ciento de los casos de malaria mexicanos.
Fue justo al sur de este estado donde en la década de los ochentas se implementó el Centro de Investigaciones del Paludismo ahora Centro Regional de Investigaciones en Salud Pública, mismo que fue impulsado por el gobierno y la OPS. “Desde este logramos conocer al parásito, cómo se transmitía y cuáles eran sus orígenes, así como evaluar métodos diagnósticos y tratamientos e incluso estudiar cuestiones genéticas y de procedencia de los parásitos de la región”.
Algunos estudios requieren trabajo internacional pues como la investigadora señaló, “este es un problema regional y no uno local. Al parásito no lo detiene ninguna frontera, como hoy lo sabemos por el SARS-CoV-2 , debemos estar preparados para los retos que se vengan”.
Sobre los trabajos de investigación mexicanos, este año Lorena González López de la Facultad de Medicina de la UNAM, comentó a la Dirección General de Divulgación de la Ciencia(7) que en el Instituto Mexicano de la Propiedad Industrial (IMPI) “hay un estudio para la generación de vacunas contra P. vivax”.
Medidas de protección

Por su parte, la investigadora del Centro Regional de Investigaciones en Salud Pública indicó que las medidas de contención dependen mucho del escenario de transmisión en una región dada. También detalló que los programas de control se componen de atención al paciente, detectando casos e incluso suministrando por adelantado tratamientos en quienes sospechan de estar enfermos en zonas de riesgo.
Los programas también requieren medidas preventivas para reducir la abundancia de mosquitos. En 2020, la OMS refirió(8) que los mosquitos tratados con insecticidas y fumigación de interiores son importantes al prevenir la enfermedad, sin embargo se ha reportado resistencia a los insecticidas entre los mosquitos Anopheles.
Según el último Informe Mundial sobre el Paludismo, 73 países reportaron esta resistencia en al menos uno de las cuatro clases de insecticidas de uso común, y 28 de estos refirieron resistencia a todas las clases principales. La eficacia de los fármacos entre las personas infectadas presenta el mismo reto.
Fuentes:
- https://direct.mit.edu/rest/article-abstract/doi/10.1162/rest_a_01050/100984/Epidemic-Shocks-and-Civil-Violence-Evidence-from?redirectedFrom=fulltext
- https://www.who.int/es/news/item/06-10-2021-who-recommends-groundbreaking-malaria-vaccine-for-children-at-risk
- https://www.who.int/es/news-room/fact-sheets/detail/malaria
- http://www.imss.gob.mx/salud-en-linea/brasil-paludismo
- https://es.gsk.com/es-es/innovación-responsable/salud-a-tu-alcance/luchando-contra-la-malaria-en-el-laboratorio-y-sobre-el-terreno/
- https://www3.paho.org/hq/index.php?option=com_docman&view=download&category_slug=datos-estadisticos-mapas-8110&alias=45385-iniciativa-e-2020-paises-hacia-eliminacion-malaria-americas-2018-385&Itemid=270&lang=es
- https://www.dgcs.unam.mx/boletin/bdboletin/2021_357.html
- https://www.who.int/es/news-room/fact-sheets/detail/malaria





Deja un comentario